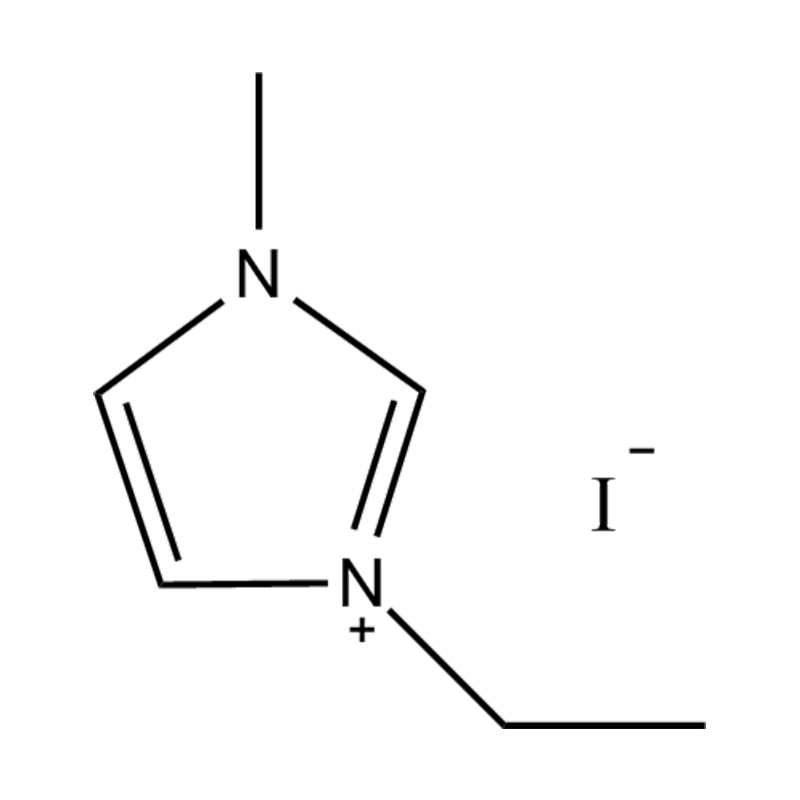
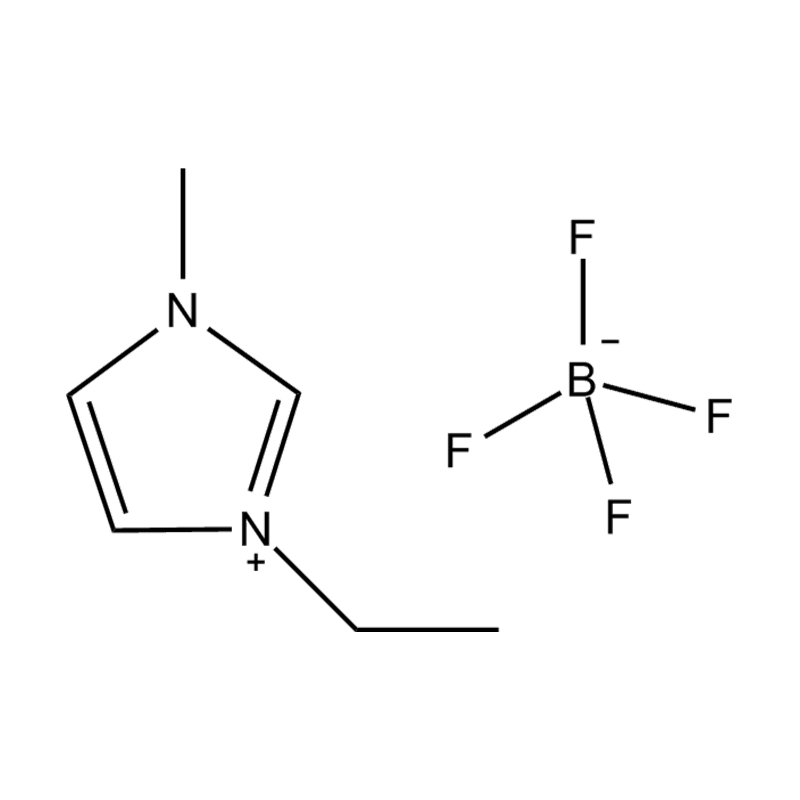
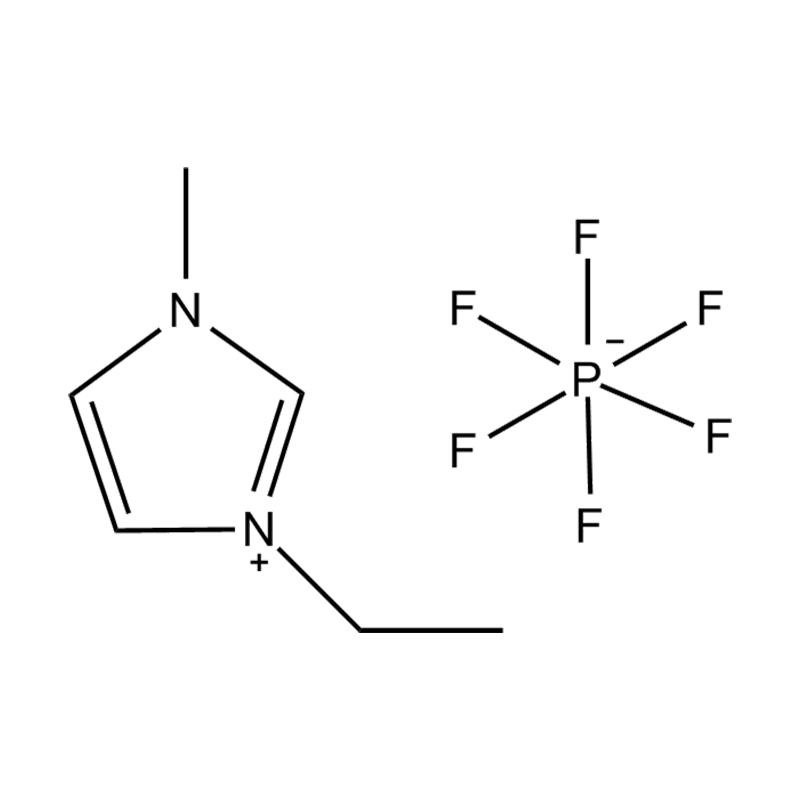
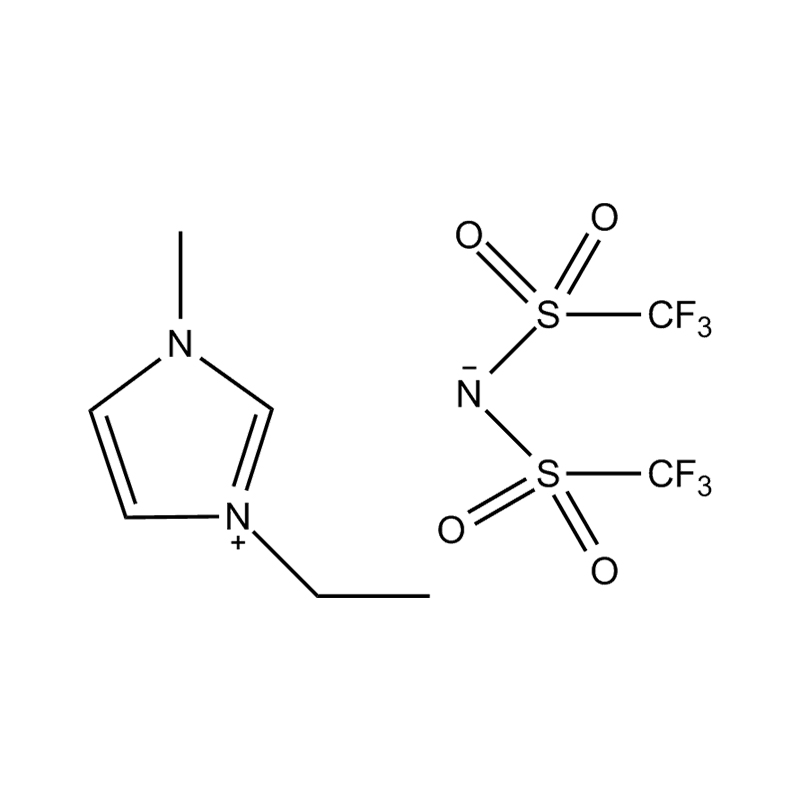
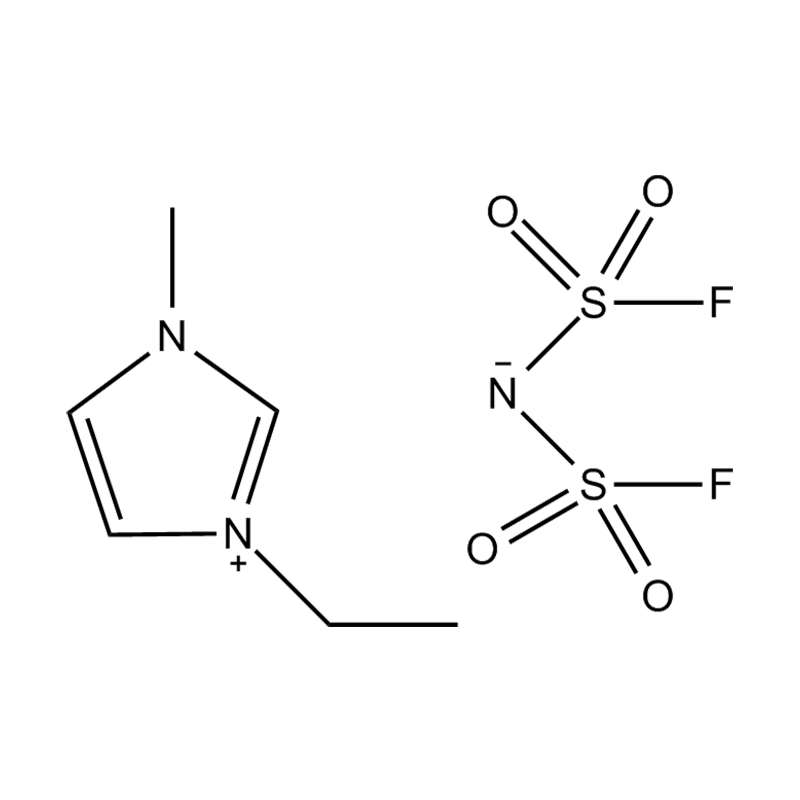
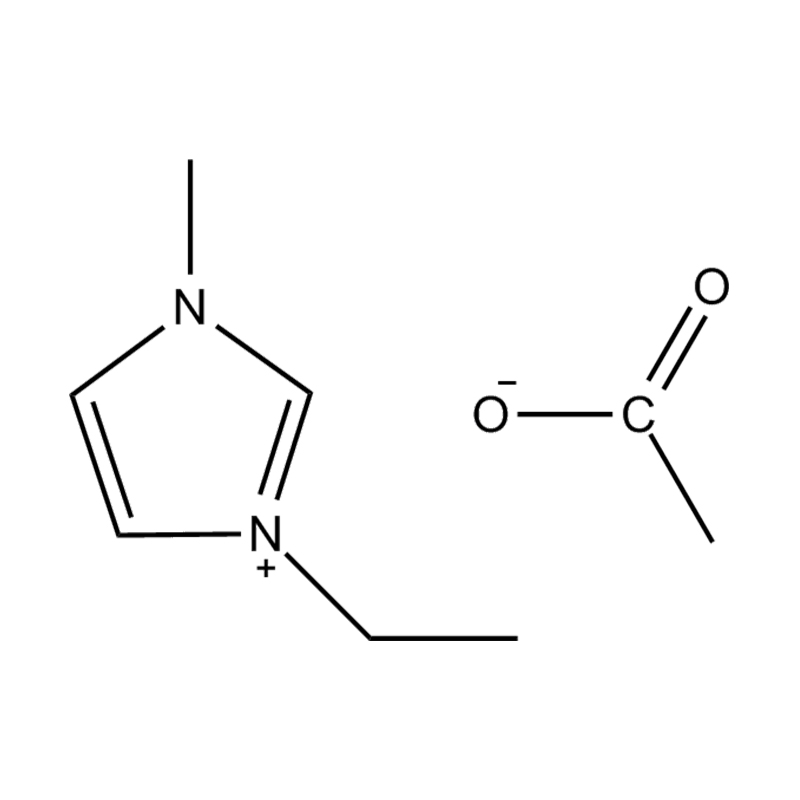
Liquides ioniques imidazole disubstitués (ILs) sont une classe spécialisée de liquides ioniques dans lesquels le cycle imidazole est remplacé à deux positions par des groupes fonctionnels. Ces modifications influencent considérablement leur propriétés physicochimiques , ce qui les rend très polyvalents pour les applications en catalyse, électrochimie, chimie verte et science des matériaux. Comprendre ces propriétés est crucial pour les chercheurs et les ingénieurs qui cherchent à exploiter les performances de ces liquides ioniques dans divers processus chimiques et industriels.
1. Viscosité
La viscosité est un paramètre clé qui affecte la comportement d'écoulement, transfert de masse et efficacité des processus de liquides ioniques. Les IL imidazole disubstitués présentent généralement :
- Viscosité modérée à élevée par rapport aux liquides ioniques d'imidazolium monosubstitués ou simples en raison de l'augmentation des interactions moléculaires provenant de substituants supplémentaires.
- Viscosité réglable : En sélectionnant soigneusement le type et la taille des substituants, la viscosité peut être ajustée pour des applications spécifiques, telles que la catalyse ou les systèmes de solvants.
- Dépendance à la température : La viscosité diminue avec l'augmentation de la température, facilitant ainsi une manipulation plus facile et un transfert de masse amélioré à des températures élevées.
Cette viscosité réglable permet aux imidazole IL disubstitués d'être utilisés comme solvants, électrolytes ou milieux réactionnels où le débit et les taux de diffusion contrôlés sont essentiels.
2. Stabilité thermique
La stabilité thermique est une propriété déterminante qui détermine la plage de température de fonctionnement des liquides ioniques :
- Stabilité thermique améliorée : Les IL imidazole disubstitués résistent généralement à des températures allant jusqu'à 300-400°C sans décomposition significative, selon les substituants et le type d'anion.
- Résistance à la dégradation : Les substituants supplémentaires peuvent fournir un obstacle stérique et stabiliser le cycle imidazole, réduisant ainsi le risque de dégradation thermique.
- Avantage d'application : La stabilité thermique élevée rend ces IL adaptés aux réactions à haute température, aux dispositifs électrochimiques et aux processus industriels dans lesquels les solvants organiques conventionnels s'évaporeraient ou se décomposeraient.
3. Conductivité ionique
La conductivité ionique est essentielle pour les applications dans électrochimie, batteries et supercondensateurs :
- Conductivité ionique modérée à élevée : Les IL imidazole disubstitués permettent une mobilité ionique efficace, avec des valeurs de conductivité influencées par la taille, la symétrie et la polarité des substituants.
- Interactions cation-anion : Les substituants modifient les interactions électrostatiques, impactant la dissociation des ions et, par conséquent, la conductivité globale.
- Effets de la température et de la viscosité : La conductivité s'améliore à des températures plus élevées en raison d'une diminution de la viscosité et d'une mobilité ionique améliorée.
Ces propriétés permettent aux imidazole IL disubstitués de servir d'électrolytes dans les dispositifs de stockage d'énergie, la galvanoplastie et la synthèse électrochimique.

4. Solubilité et polarité
La présence de deux substituants sur le cycle imidazole modifie les caractéristiques de solubilité et de polarité :
- Solubilité améliorée : Selon les groupes fonctionnels, ces IL peuvent dissoudre un large éventail de substances organiques, inorganiques et polymères.
- Polarité réglable : Les substituants peuvent augmenter ou diminuer la polarité globale du liquide ionique, en l'adaptant à des solvants ou des milieux réactionnels spécifiques.
- Compatibilité avec les catalyseurs : Le profil de solubilité permet aux imidazole IL disubstitués de soutenir une catalyse homogène et de stabiliser les complexes métalliques.
5. Diverses propriétés physicochimiques
Les propriétés supplémentaires influencées par la disubstitution comprennent :
- Hydrophobie ou hydrophilie : Les substituants peuvent faire passer le liquide ionique de soluble dans l'eau à non miscible à l'eau, permettant ainsi des systèmes de solvants sélectifs.
- Densité et tension superficielle : Les modifications apportées au cycle imidazole affectent le tassement et les interactions intermoléculaires, influençant la densité et le comportement interfacial.
- Fenêtre électrochimique : Les IL disubstituées présentent souvent fenêtres électrochimiques plus larges , permettant leur utilisation dans des applications électrochimiques haute tension.
6. Implications pratiques
Les propriétés physicochimiques uniques des liquides ioniques imidazole disubstitués les rendent adaptés à une variété d'applications :
- Solvants verts : Leur stabilité thermique, leur faible volatilité et leur polarité réglable leur permettent de remplacer les solvants organiques volatils dans les processus respectueux de l'environnement.
- Électrolytes : Une conductivité ionique élevée et de larges fenêtres électrochimiques les rendent idéales pour les batteries, les piles à combustible et les supercondensateurs.
- Catalyse : La solubilité et la viscosité réglables optimisent les conditions de réaction et améliorent l’efficacité du catalyseur.
- Synthèse des matériaux : La stabilisation des nanoparticules et des polymères dans les liquides ioniques est facilitée par des interactions cation-anion adaptées.
Conclusion
Les liquides ioniques imidazole disubstitués présentent une combinaison de viscosité réglable, stabilité thermique élevée, excellente conductivité ionique et solubilité réglable , ce qui en fait des outils polyvalents dans la chimie et l’ingénierie modernes. En sélectionnant les substituants et les contre-ions appropriés, les chercheurs peuvent concevoir des liquides ioniques répondant à des exigences spécifiques pour chimie verte, électrochimie, catalyse et science des matériaux . Leurs propriétés physicochimiques uniques améliorent non seulement l'efficacité des processus, mais contribuent également au développement de systèmes chimiques plus durables et plus performants.



 中文简体
中文简体