Liquides ioniques pyridine (PIL), parmi les générations précédentes de liquides ioniques étudiés, ont attiré l'attention pour leur simplicité structurelle et leurs propriétés réglables. Composés d'un cation pyridinium et d'une gamme diversifiée d'anions, ces composés offrent une plateforme polyvalente pour explorer la chimie fondamentale des liquides ioniques. Cependant, l'application pratique des PIL a été limitée par certaines limitations physico-chimiques, notamment leurs points de fusion relativement élevés. Cet article examine les principales relations structure-propriété qui définissent le comportement des PIL et évalue leur potentiel dans diverses applications chimiques et industrielles.
Caractéristiques structurelles
La caractéristique déterminante des liquides ioniques pyridine réside dans leur structure cationique. Le cation est généralement un ion N-alkylpyridinium, où la longueur de la chaîne alkyle peut varier (par exemple, éthyle, butyle, hexyle ou octyle). La nature de ce substituant influence directement les propriétés physiques du liquide ionique résultant, telles que la viscosité, la stabilité thermique et le point de fusion. Des chaînes alkyles plus courtes entraînent généralement des interactions ioniques plus fortes et une cristallinité accrue, conduisant à des points de fusion plus élevés. En revanche, des chaînes plus longues augmentent le caractère hydrophobe et peuvent supprimer la cristallinité, abaissant potentiellement le point de fusion.
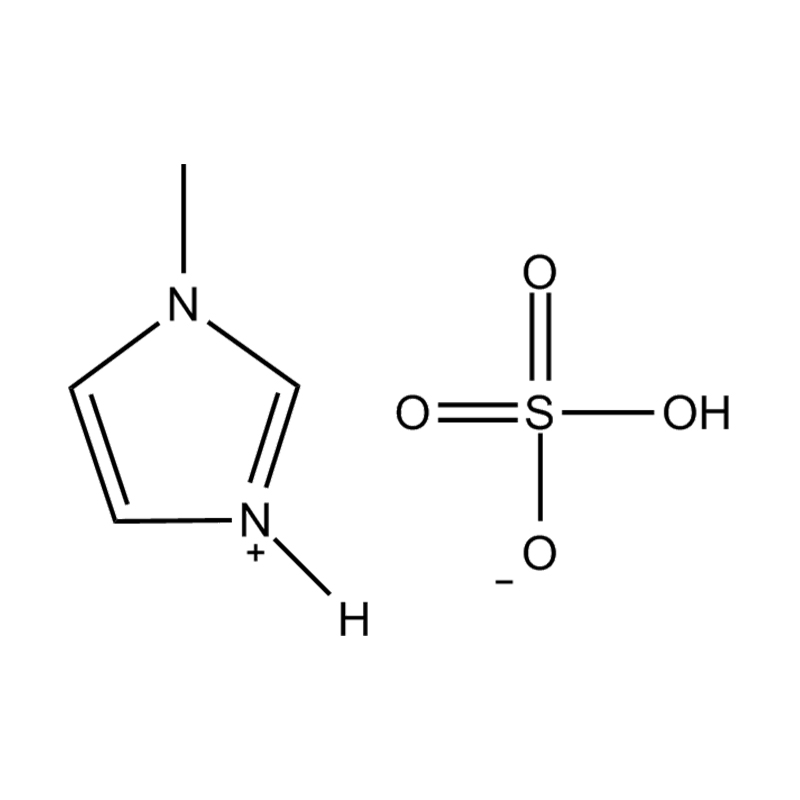
Du côté anionique, les PIL incorporent une large gamme de contre-ions, notamment :
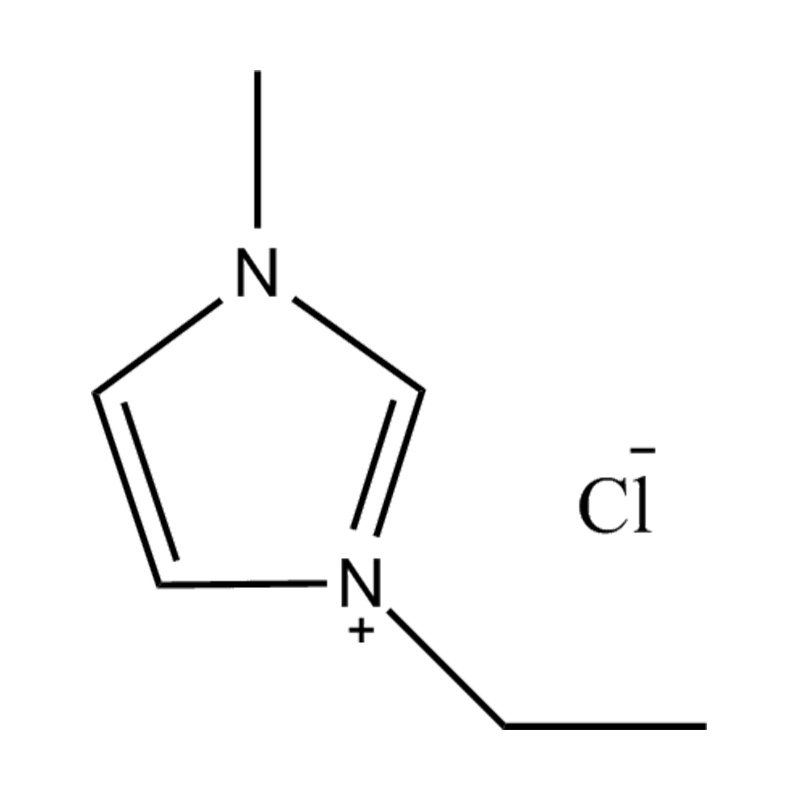
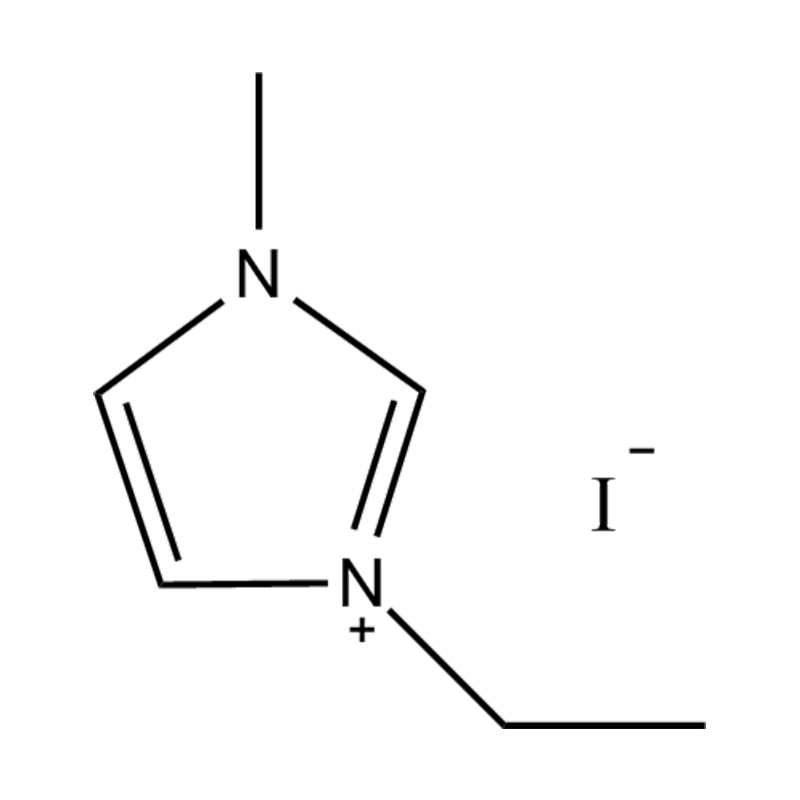
Halogénures : chlorure (Cl⁻), bromure (Br⁻)
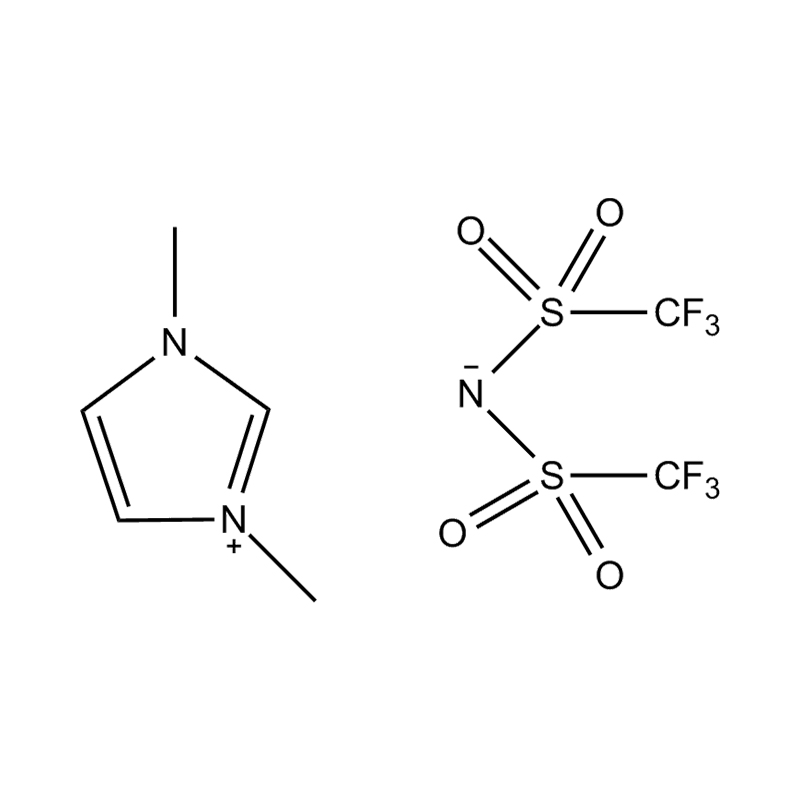
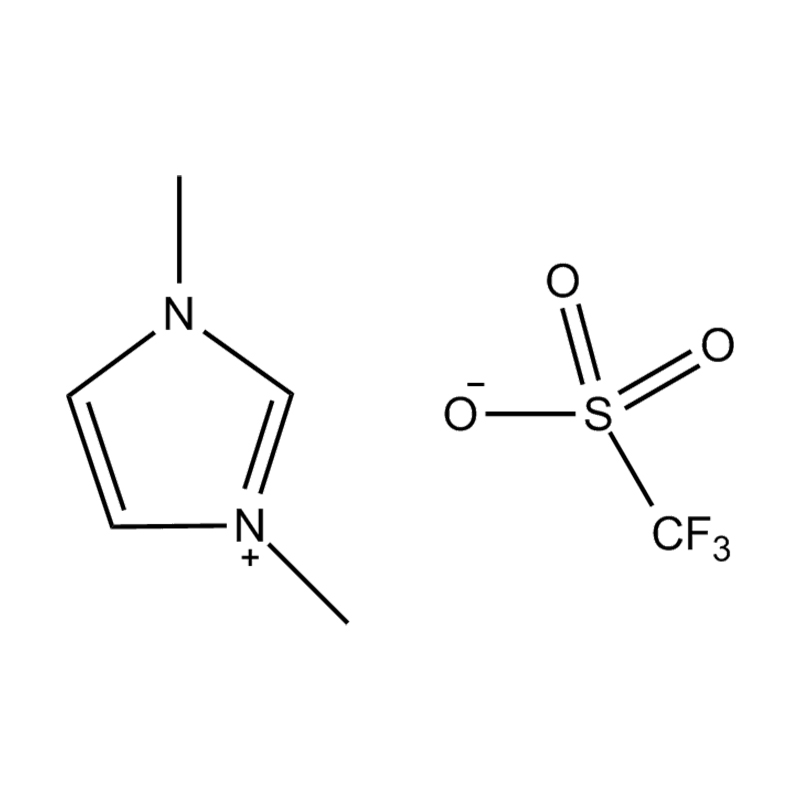
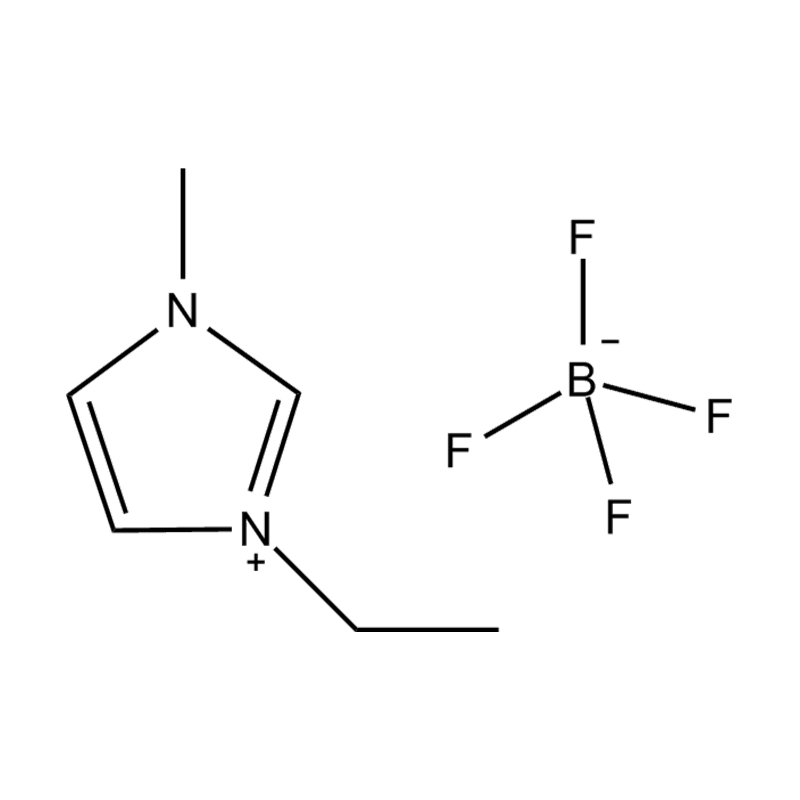
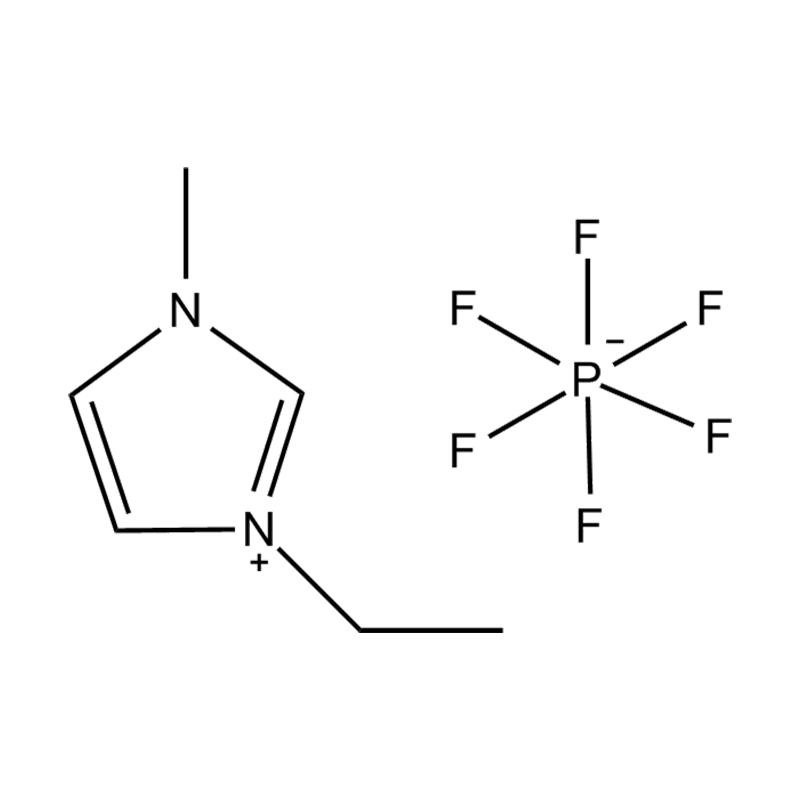
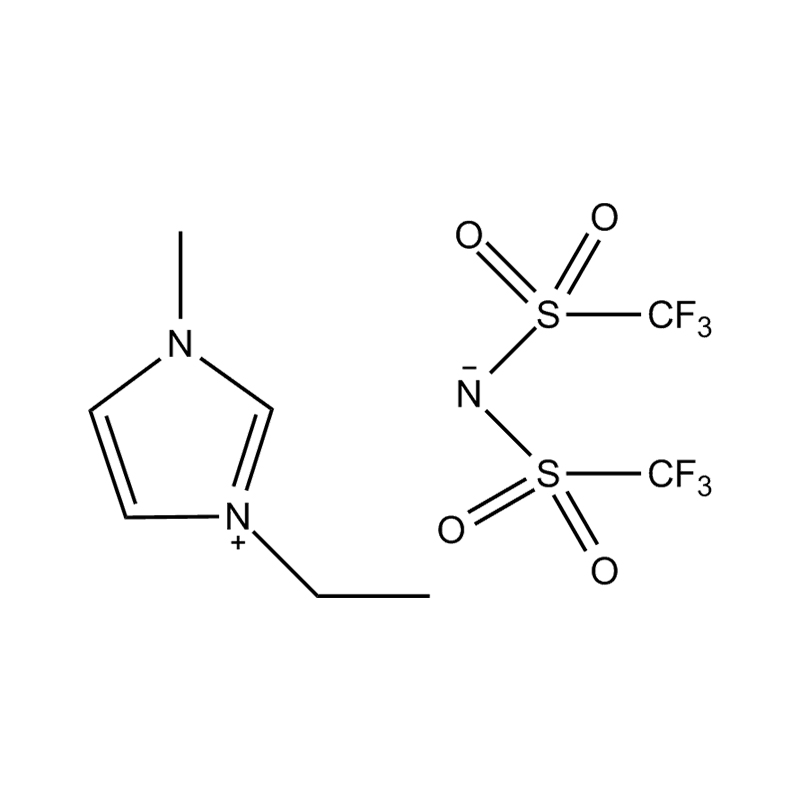
Anions fluorés : tétrafluoroborate (BF₄⁻), hexafluorophosphate (PF₆⁻), bis(trifluorométhanesulfonyl)imide (NTf₂⁻)
Chaque anion confère des caractéristiques thermiques, chimiques et solvatantes spécifiques. Par exemple, NTf₂⁻ est connu pour conférer une faible viscosité et une stabilité thermique élevée, ce qui le rend particulièrement attrayant pour les systèmes hydrophobes et à haute température.
Propriétés physicochimiques
Les propriétés physicochimiques des PIL sont étroitement liées à l’interaction entre le cation et l’anion. Le point de fusion, souvent supérieur à celui d’autres liquides ioniques courants tels que les dérivés d’imidazolium ou de pyrrolidinium, est un facteur limitant critique. Ceci est largement attribué à la nature aromatique planaire du cycle pyridinium, qui favorise un fort empilement π-π et un emballage ordonné à l'état solide.
Malgré cela, les liquides ioniques pyridine présentent des caractéristiques favorables à plusieurs égards :
Stabilité thermique : De nombreux PIL se décomposent à des températures supérieures à 200°C, ce qui les rend adaptés aux applications à haute température.
Fenêtre électrochimique : Ils présentent souvent une large fenêtre électrochimique, importante pour les applications électrochimiques.
Capacité de solvatation : selon l'anion, les PIL peuvent dissoudre une gamme de substances organiques, inorganiques et polymères.
Relations structure-propriété
Comprendre les relations structure-propriété dans les PIL est crucial pour adapter leur comportement à des tâches spécifiques. Les relations clés comprennent :
Longueur de la chaîne alkyle par rapport à la viscosité et au point de fusion : L'augmentation de la longueur de la chaîne alkyle réduit généralement le point de fusion mais augmente la viscosité.
Type d'anion par rapport à l'hydrophobicité et à la stabilité : les anions fluorés tels que PF₆⁻ et NTf₂⁻ améliorent la stabilité thermique et électrochimique, tandis que les halogénures offrent une conductivité plus élevée mais une robustesse thermique inférieure.
Planarité des cations par rapport à l'emballage à l'état solide : La nature planaire du cycle pyridinium contribue à des points de fusion plus élevés en raison d'une formation de réseau ionique plus forte.
Champ d'application
Bien qu’ils ne soient pas aussi largement utilisés que d’autres liquides ioniques, les liquides ioniques à base de pyridine ont montré leur potentiel dans plusieurs niches et domaines émergents :
Systèmes électrochimiques
En raison de leur conductivité ionique et de leur stabilité électrochimique, les PIL sont candidats comme électrolytes dans les batteries, les condensateurs et les piles à combustible. L'accordabilité des structures cationiques et anioniques permet une optimisation dans des régimes de tension et de conductivité spécifiques.
Catalyse et milieux de réaction
Les PIL ont été étudiés en tant que solvants et co-catalyseurs dans les réactions organiques, en particulier dans les transformations bénéficiant de milieux ioniques à faible volatilité et à bonne endurance thermique.
Technologies d'extraction et de séparation
La solubilité sélective des PIL permet leur utilisation dans les systèmes d’extraction liquide-liquide d’ions métalliques, de polluants organiques et de biomolécules.
Traitement des matériaux et polymérisation
Certaines études explorent les PIL en tant que solvants ou additifs dans les réactions de polymérisation, bénéficiant de leur polarité et de leurs propriétés thermiques.
Défis et perspectives
Le principal défi limitant une adoption plus large des PIL reste leur point de fusion relativement élevé, en particulier pour ceux comportant de courtes chaînes alkyle et des anions halogénures simples. Les stratégies pour résoudre ce problème incluent l'utilisation de groupes alkyles asymétriques, l'incorporation d'anions volumineux ou flexibles et la synthèse de mélanges ou de systèmes eutectiques à base de PIL.
Les développements futurs pourraient également se concentrer sur la fonctionnalisation du cycle pyridinium avec des groupes réactifs ou de coordination supplémentaires pour permettre des interactions spécifiques en catalyse, en détection ou en reconnaissance moléculaire. Avec la demande croissante de solvants inoffensifs pour l’environnement et de structure diversifiée, un regain d’intérêt pour les liquides ioniques à base de pyridine est attendu.
Les liquides ioniques à base de pyridine offrent une classe de composés structurellement riches et fonctionnellement réglables au sein de la famille plus large des liquides ioniques. Bien que leur utilisation soit actuellement limitée par les propriétés thermiques, les recherches en cours sur l’optimisation des propriétés structurels pourraient ouvrir la voie à une gamme d’applications plus large. Leurs caractéristiques électrochimiques uniques, leur comportement de solvatation et leur conception modulaire en font des candidats prometteurs pour des applications spécialisées en électrochimie, catalyse et traitement des matériaux.



 中文简体
中文简体