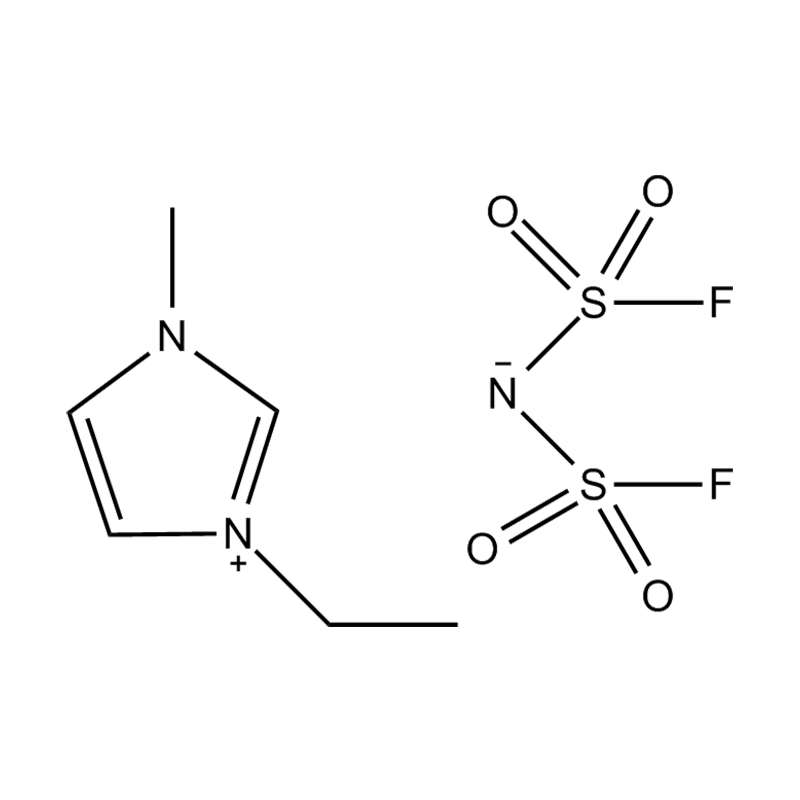
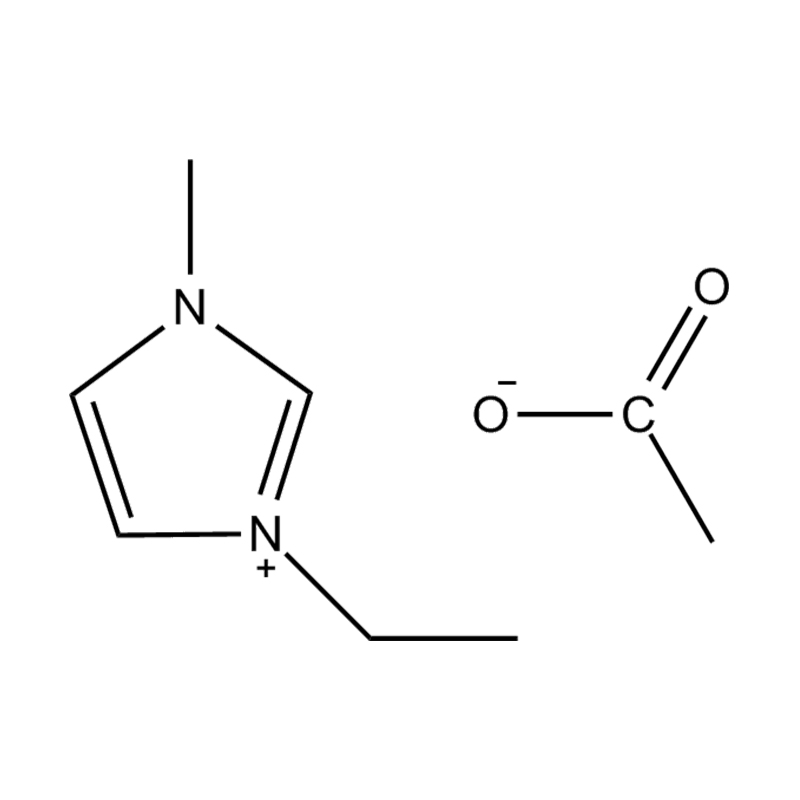
La stabilité électrochimique de liquides ioniques imidazole disubstitués dans des environnements à haute tension ou à activité redox est influencé par plusieurs mécanismes interdépendants ancrés dans leur structure moléculaire et leur configuration électronique :
Délocalisation des électrons sur le cycle imidazole : La nature aromatique du cycle imidazole permet une délocalisation significative des électrons π, ce qui améliore la résistance de la molécule à la dégradation oxydative ou réductrice. Lorsqu'elle est substituée aux positions 1 et 3, la densité électronique peut être redistribuée de manière à stabiliser le cation contre les réactions de transfert d'électrons.
Effets des substituants : Le type et la position des substituants sur le cycle imidazole affectent de manière significative la stabilité électrochimique. Les groupes donneurs d'électrons peuvent améliorer la nucléophilie et réduire la stabilité oxydative, tandis que les groupes attracteurs d'électrons (tels que les halogènes ou les nitriles) peuvent améliorer la résistance à l'oxydation en stabilisant l'orbitale moléculaire occupée la plus élevée (HOMO). À l’inverse, ces groupes peuvent également réduire le potentiel de réduction en stabilisant l’orbitale moléculaire la plus basse inoccupée (LUMO), en fonction de l’environnement.

Entrave stérique et protection spatiale : des substituants volumineux en positions 1 et 3 peuvent protéger physiquement le cycle imidazolium des attaques nucléophiles ou électrophiles, limitant ainsi les réactions secondaires indésirables qui pourraient se produire dans des conditions de haute tension.
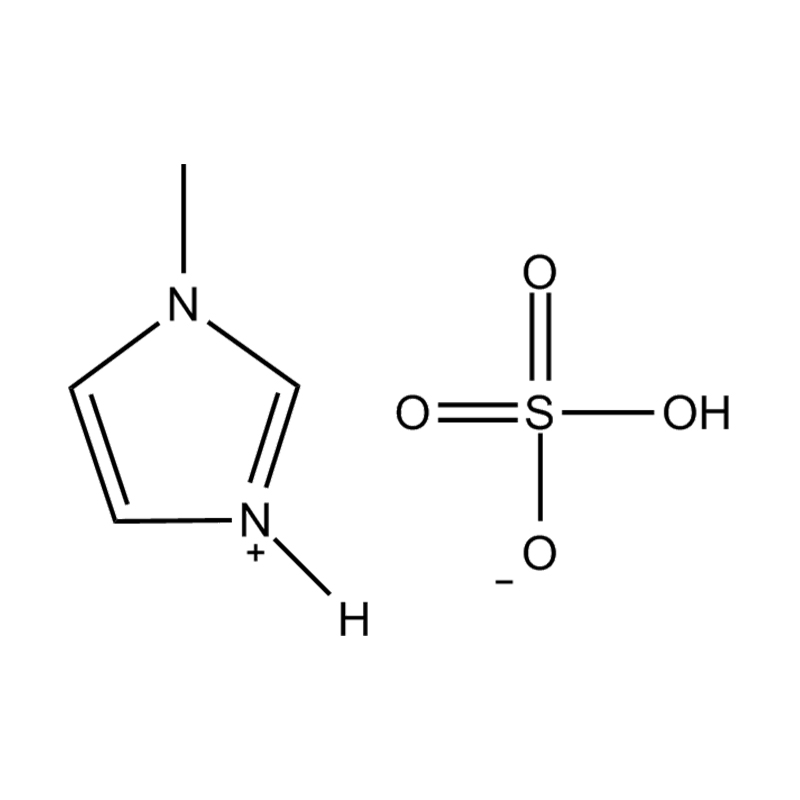
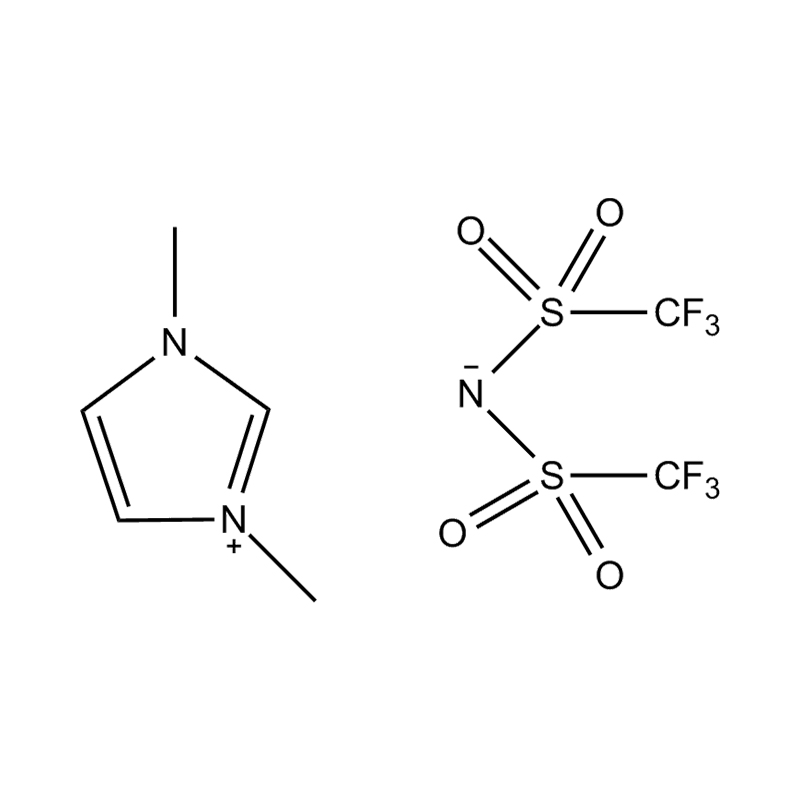
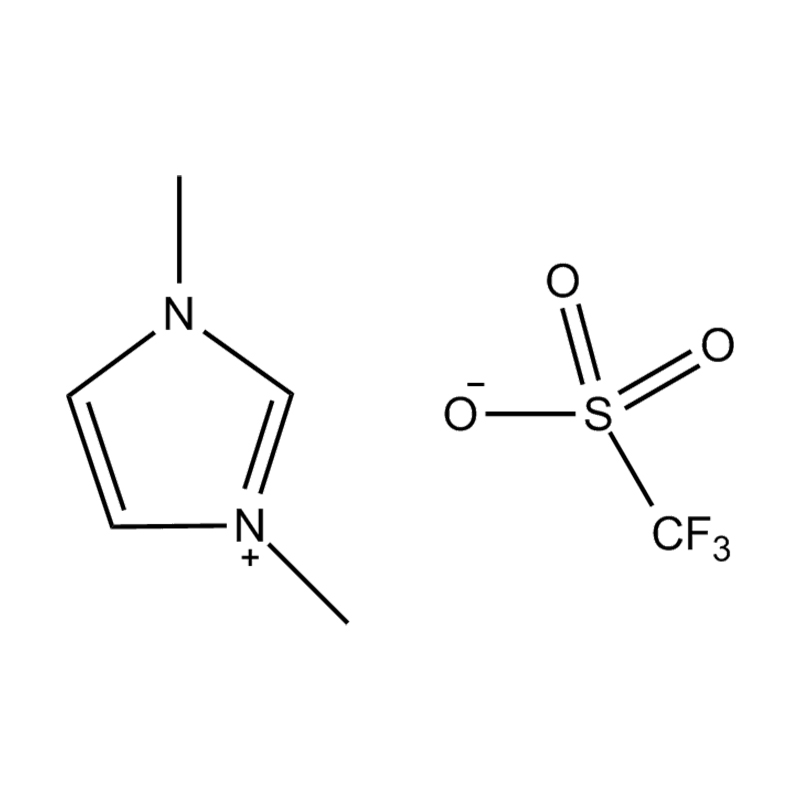
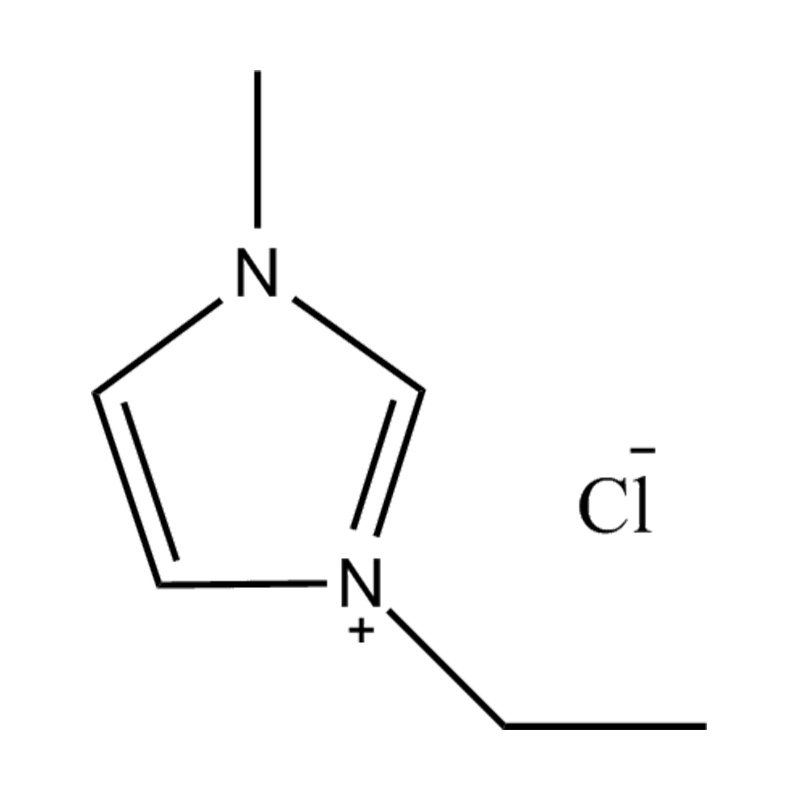
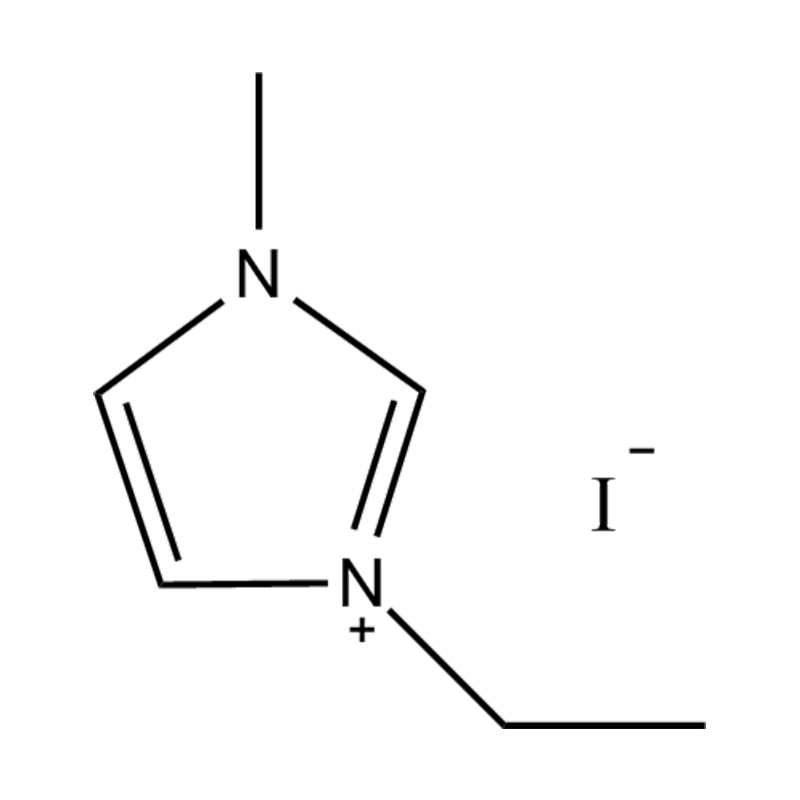
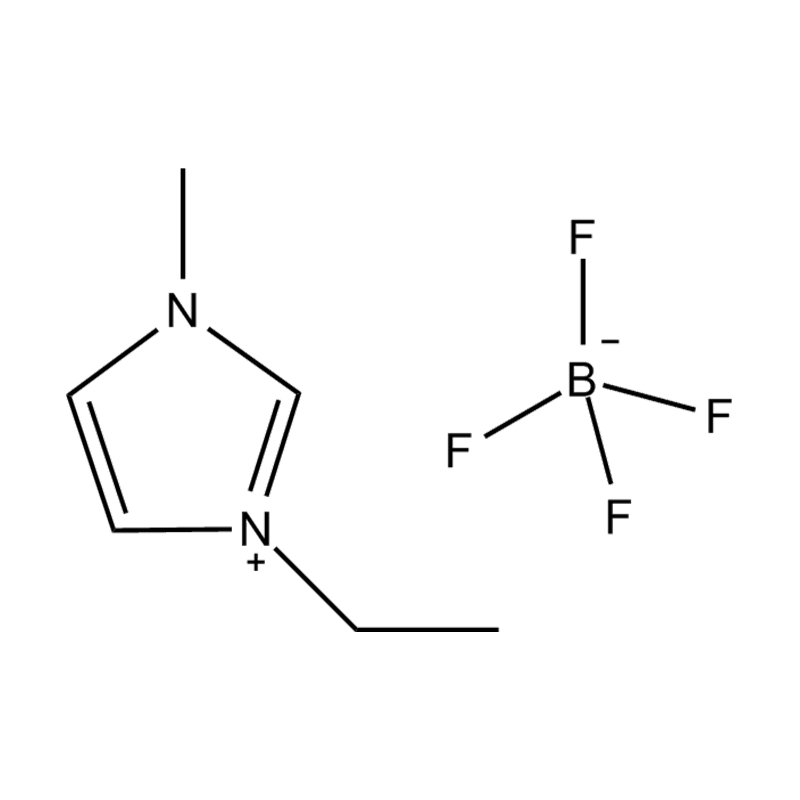
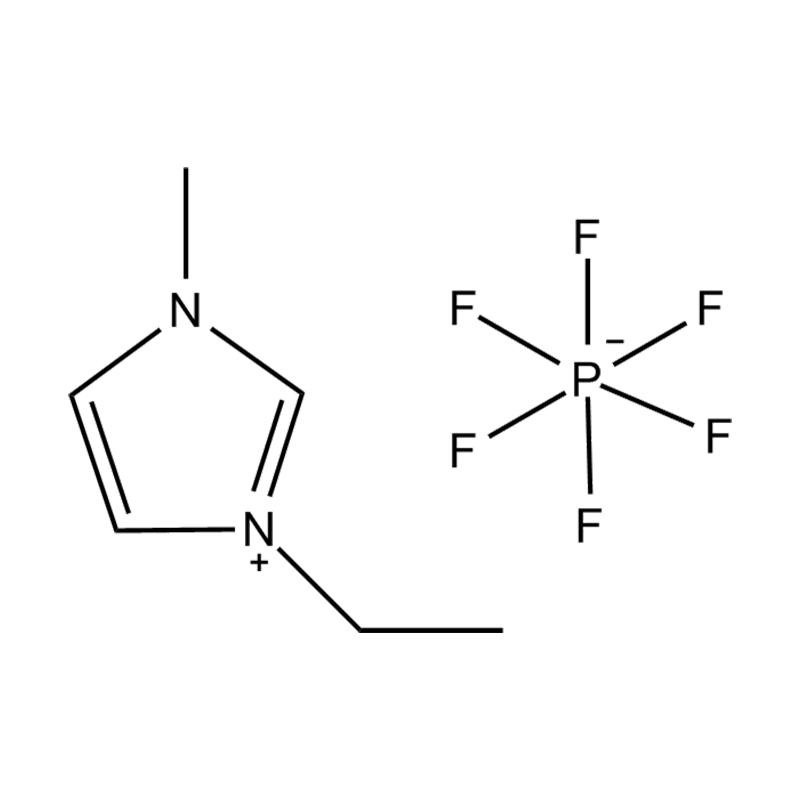
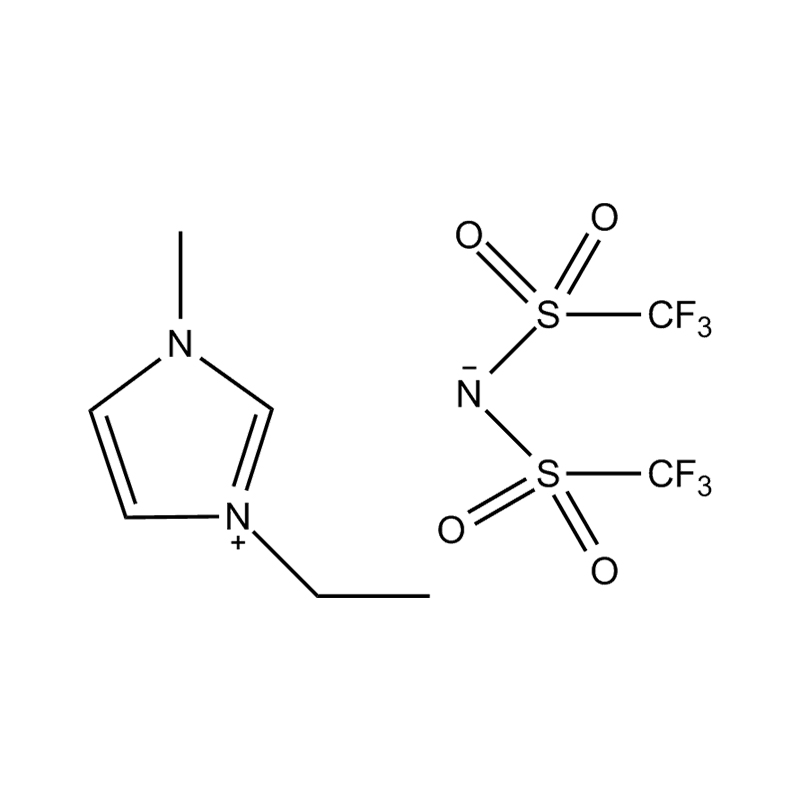
Stabilité de la paire anion-cation : l'appariement du cation imidazolium disubstitué avec un anion stable et non coordinateur (par exemple, le bis(trifluorométhylsulfonyl)imide [TFSI⁻] ou le tétrafluoroborate [BF₄⁻]) réduit le risque de réactions secondaires et contribue à une fenêtre électrochimique plus large. Ces anions résistent à la décomposition et maintiennent la conductivité ionique sans interférer dans les réactions redox.
Mobilité ionique et comportement interfacial : dans les systèmes à haute tension, en particulier dans les dispositifs électrochimiques, la mobilité des ions et leur organisation aux interfaces des électrodes influencent la stabilité. Les liquides ioniques imidazole disubstitués peuvent former des couches interfaciales bien organisées qui empêchent le transfert direct d'électrons entre l'électrode et les espèces ioniques, améliorant ainsi leur fenêtre électrochimique.
Stabilité thermique et voies de décomposition : La stabilité thermique intrinsèque de la structure de l'imidazole disubstitué minimise le risque de décomposition thermique sous contrainte électrochimique, qui s'accompagne souvent d'une dégradation induite par la tension.



 中文简体
中文简体