Dans le paysage en constante évolution des matériaux avancés, liquides ioniques (IL) sont apparus comme une classe révolutionnaire de substances qui défient les catégorisations conventionnelles des liquides, des sels et des solvants. Mais qu’est-ce qui rend exactement les liquides ioniques si uniques et pourquoi sont-ils de plus en plus considérés comme une pierre angulaire du développement de technologies durables, de chimie verte et de systèmes électrochimiques de nouvelle génération ?
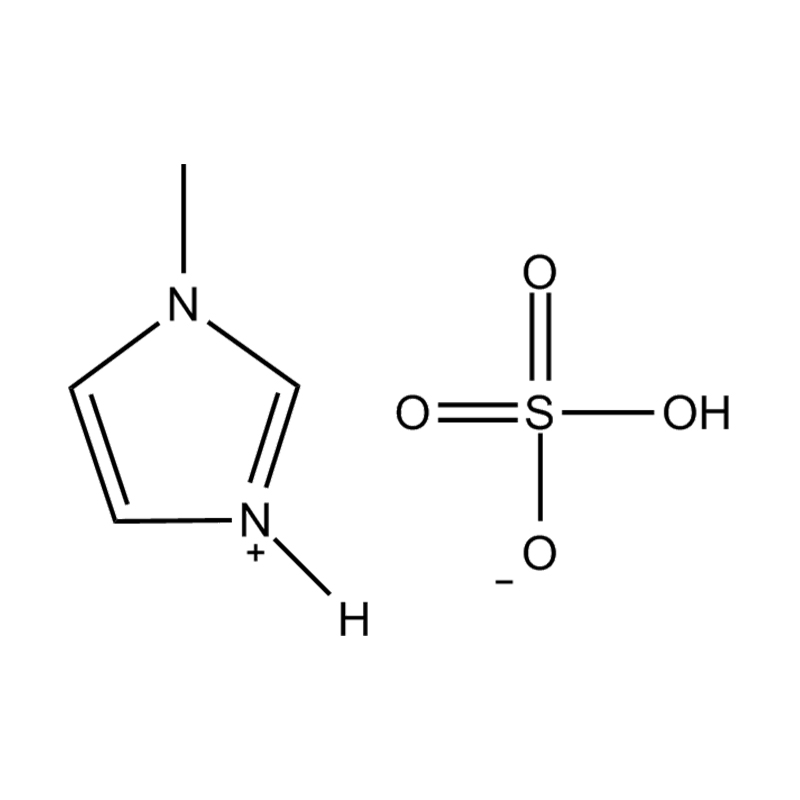
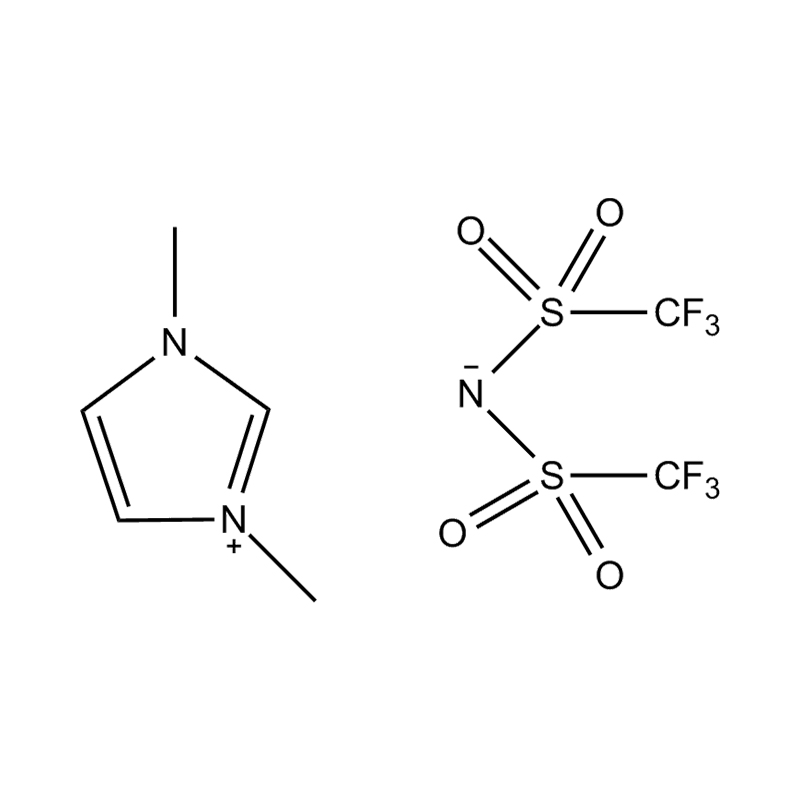
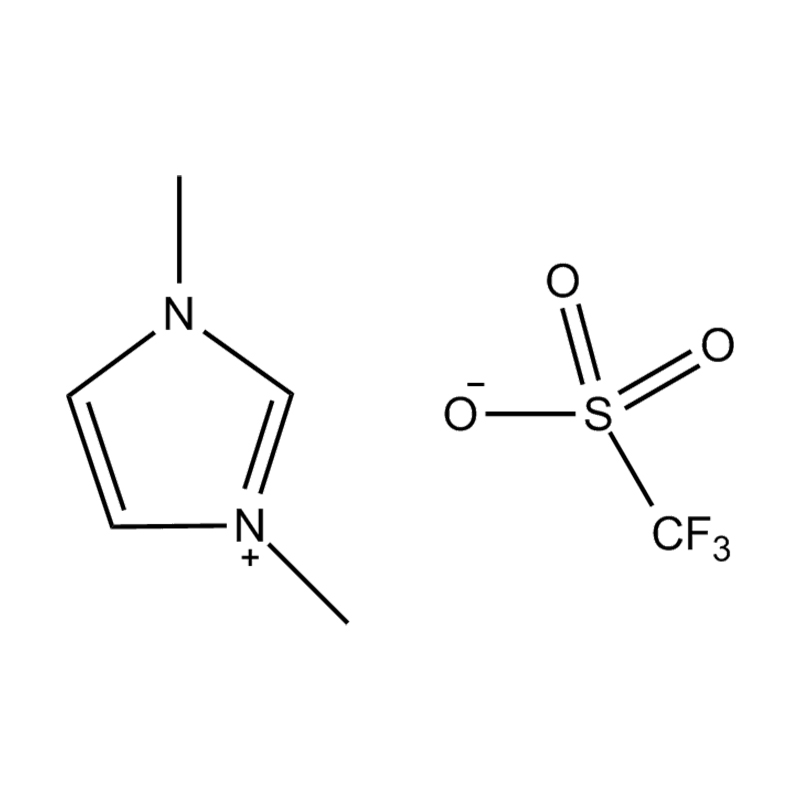
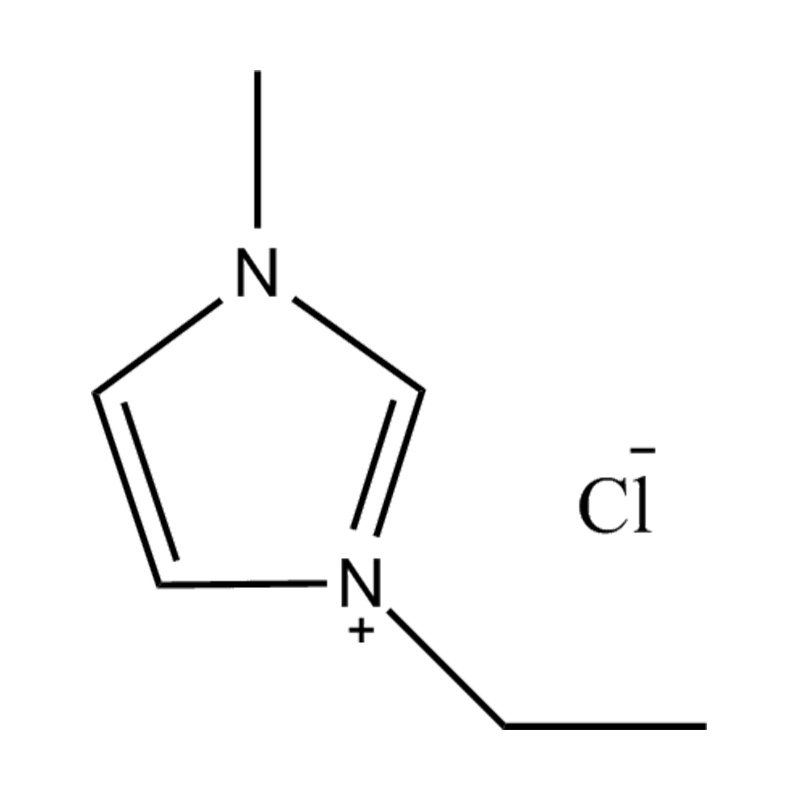
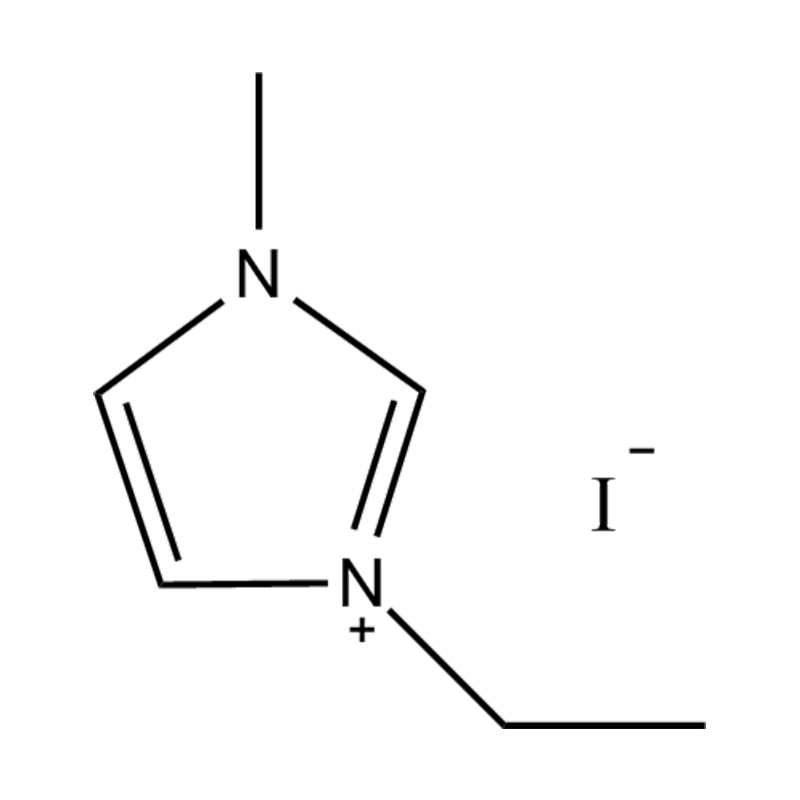
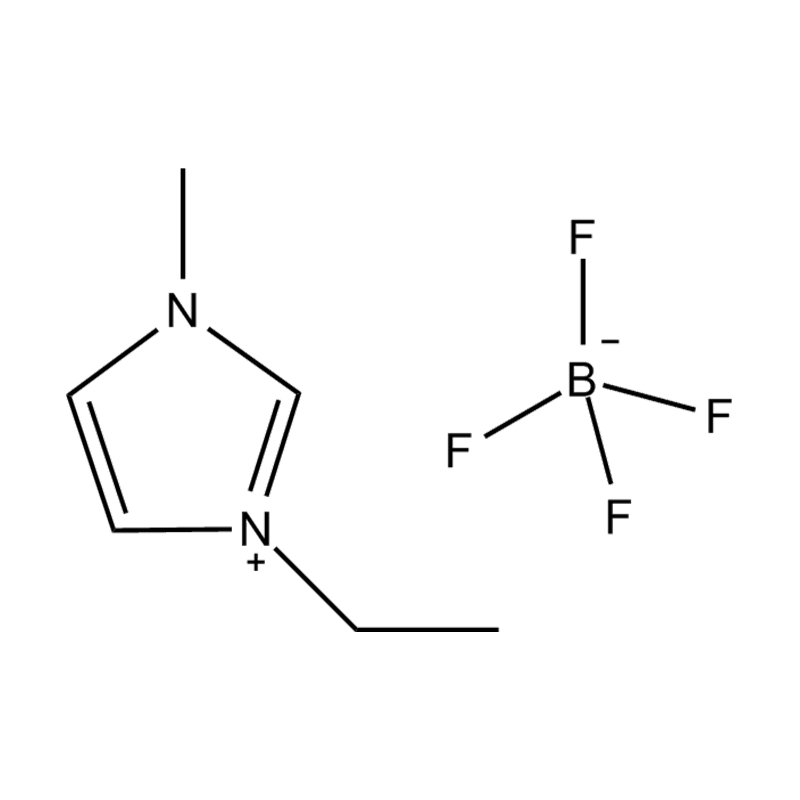
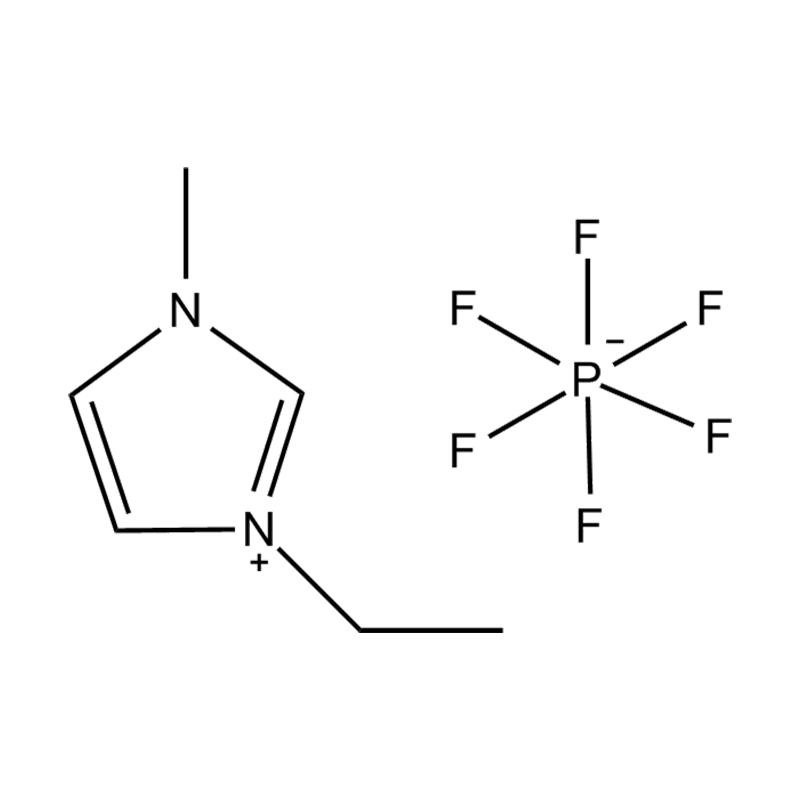
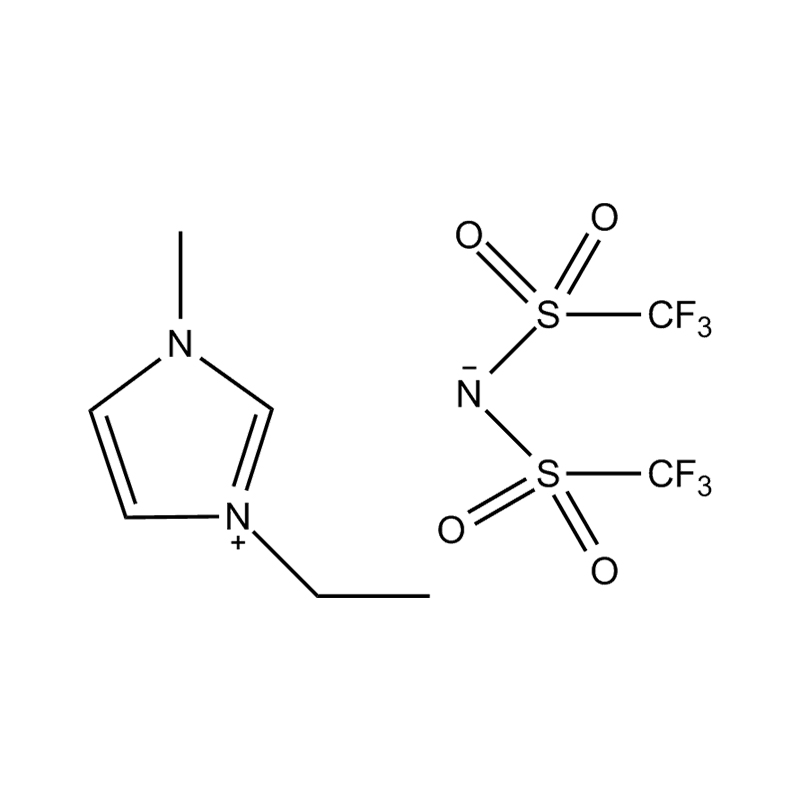
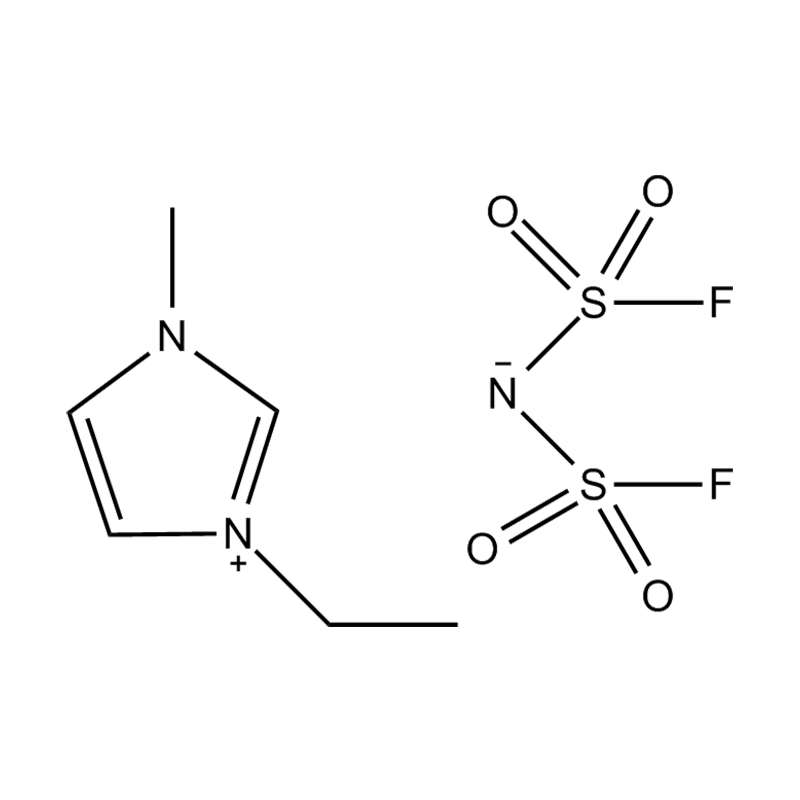
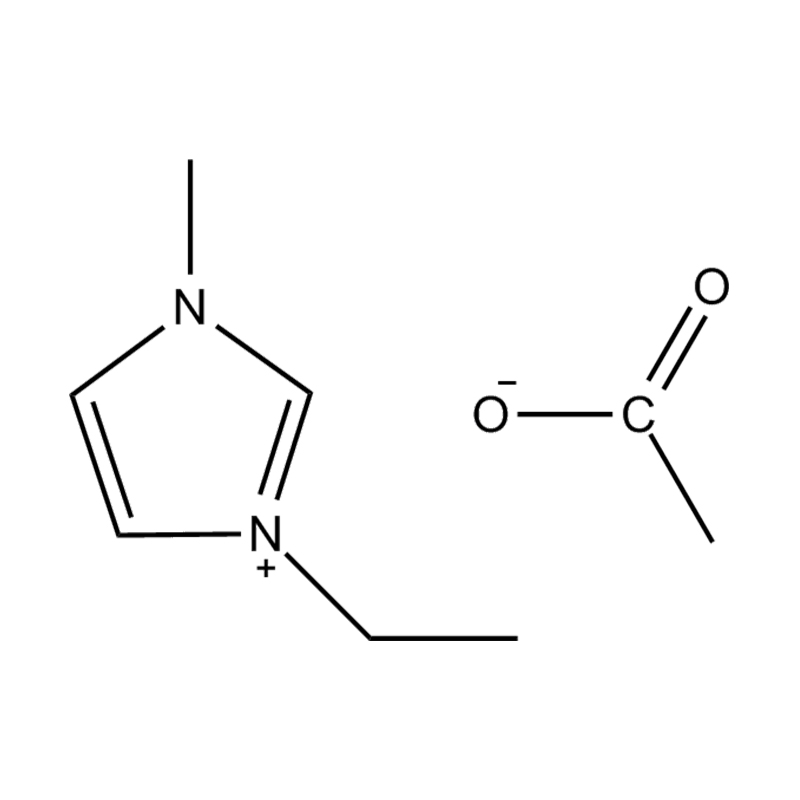
Au niveau le plus fondamental, un liquide ionique est un sel composé entièrement d'ions qui reste à l'état liquide en dessous de 100°C, souvent même à température ambiante. Contrairement aux sels traditionnels tels que le chlorure de sodium, qui nécessitent des températures élevées pour fondre, les liquides ioniques sont généralement fabriqués à partir de cations organiques volumineux et asymétriques (comme l'imidazolium, le pyridinium, l'ammonium) associé à anions inorganiques ou organiques (comme le bis(trifluorométhylsulfonyl)imide, PF₆⁻, BF₄⁻ ou des halogénures). Les formes irrégulières et la faible coordination entre les ions empêchent la cristallisation et entraînent leurs points de fusion bas caractéristiques.
Les propriétés physicochimiques des liquides ioniques sont aussi diverses que leurs structures moléculaires accordables. L'un de leurs traits les plus déterminants est pression de vapeur négligeable , ce qui les rend non volatils et donc attrayants comme alternatives respectueuses de l'environnement aux solvants organiques traditionnels. Cette fonctionnalité à elle seule les a placés à l'avant-garde initiatives de chimie verte , où l'élimination des composés organiques volatils (COV) est une priorité.
En plus d'être non volatils, les liquides ioniques présentent stabilité thermique et électrochimique exceptionnelle . De nombreux IL peuvent fonctionner à des températures supérieures à 200°C sans se décomposer, et leurs larges fenêtres électrochimiques (jusqu'à 6 V dans certains systèmes) en font des électrolytes idéaux dans des applications telles que batteries lithium-ion, supercondensateurs et placage métallique . Leur nature ionique intrinsèque confère également une conductivité ionique élevée, en particulier dans les systèmes où les solvants conventionnels s'évaporeraient ou se dégraderaient dans des conditions difficiles.
Un autre avantage essentiel des liquides ioniques réside dans leur accordabilité chimique . En modifiant le cation ou l'anion, les scientifiques peuvent affiner des propriétés telles que la viscosité, la polarité, l'hydrophilie ou encore la capacité de coordination. Cela a permis la création de liquides ioniques spécifiques à une tâche (TSIL) conçu pour des rôles très sélectifs, par exemple dans le captage du CO₂, le traitement de la biomasse ou la catalyse des métaux de transition. La modularité des IL en fait une sorte de « solvant design » pour les environnements chimiques complexes.
Dans le domaine de séparations et extractions , les liquides ioniques offrent plusieurs avantages par rapport aux solvants traditionnels. Leur capacité à solubiliser une large gamme de composés organiques et inorganiques, associée à leur immiscibilité avec l'eau ou les hydrocarbures (selon la composition), permet des systèmes d'extraction liquide-liquide très efficaces. Les IL ont été utilisés pour récupération des éléments des terres rares, élimination des composés soufrés des carburants et même extraction de molécules bioactives des plantes .
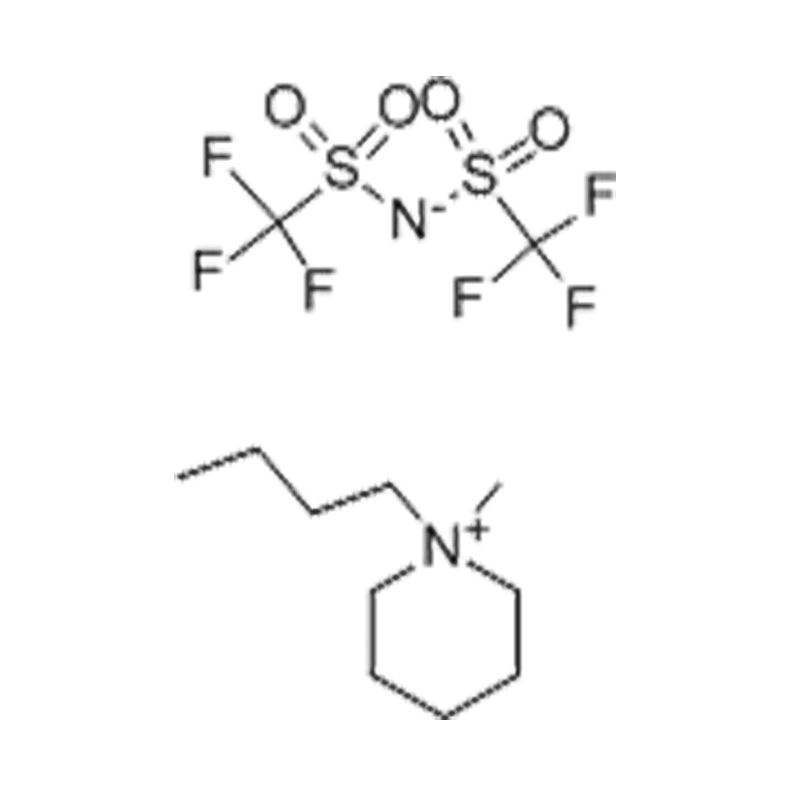
Dans catalyse , à la fois en tant que solvants et cocatalyseurs, les IL améliorent la sélectivité et le rendement de la réaction tout en simplifiant la séparation des produits. De nombreux complexes de métaux de transition présentent une stabilité et une activité améliorées dans les milieux IL. Notamment, les liquides ioniques ont été utilisés dans réactions asymétriques d'hydrogénation, d'alkylation et de couplage croisé , souvent dans des conditions plus douces que dans les systèmes conventionnels.
L'une des applications les plus avancées des liquides ioniques se situe dans le domaine de dispositifs électrochimiques et stockage d'énergie . Des électrolytes à base d'IL sont incorporés dans batteries au lithium métal, batteries sodium-ion, cellules solaires sensibilisées aux colorants (DSSC) et même électrolytes à l'état solide . Leur inertie électrochimique, leur ininflammabilité et leur tolérance thermique offrent des avantages essentiels pour améliorer à la fois la sécurité et les performances des systèmes énergétiques.
Malgré leur promesse, les liquides ioniques ne sont pas sans défis. De nombreuses IL sont encore coûteuses à synthétiser à grande échelle, et certaines souffrent de haute viscosité , ce qui limite les taux de transfert de masse. De plus, même si les LI sont souvent présentés comme des « solvants verts », leur biodégradabilité et toxicité varient considérablement en fonction de la structure, et l’impact environnemental à long terme reste un domaine de recherche actif. Répondre à ces préoccupations par des voies de synthèse plus durables et une analyse complète du cycle de vie sera essentiel pour une adoption plus large.
L’avenir des liquides ioniques est de plus en plus interdisciplinaire. Dans science des matériaux , les IL sont utilisés comme solvants et modèles dans la synthèse de nanomatériaux, de structures métallo-organiques (MOF) et de polymères conducteurs. Dans biotechnologie , ils permettent la stabilisation des enzymes, l’extraction des protéines et même la manipulation de l’ADN dans des conditions non traditionnelles. Leur rôle potentiel dans captage et utilisation du carbone (CCU) Les technologies prennent également de l’ampleur, notamment compte tenu de leur affinité pour le CO₂ et de leur haute résistance thermique.



 中文简体
中文简体